2025年3月20日,南京财经大学食品科学与工程学院2021级硕士研究生马赛(第一作者),马高兴教授(通讯作者)在国际TOP期刊Journal of Agricultural and Food Chemistry (Q1,IF: 5.7)发表题为“Effects and Mechanisms of Pleurotus eryngii Polysaccharide on Intestinal Barrier Damage: Based on the Perspective of Its Interaction with Intestinal Mucus during Gut Digestion”的研究性论文。
杏鲍菇多糖(Pleurotus eryngii polysaccharides, PEPs)是一种具有丰富功能活性的食源性菌物多糖,研究初期,团队深入分析了具PEPs的免疫调节活性,并研究了PEPs在体内和体外的消化和发酵特性,进而利用葡聚糖硫酸钠(DSS)诱导的小鼠肠炎模型观察了PEPs与肠道微生物群之间的相互作用对结肠炎的改善作用,但并未对相关机制进行深入解析。
当前,关于肠道第一道屏障,肠粘液(IMs)层对PEPs活性的影响研究较少。具体而言,由于PEPs结构和代谢过程的复杂性,以及PEPs必须通过各种肠道屏障才能接触细胞或进入循环系统,因此有必要研究它们在肠道粘液层中的行为和变化。团队前期研究分析了PEPs和IMs在体外相互作用的理化性质,并鉴于物质结构与功能之间的关系,初步发现了与IMs的相互作用可能会影响PEPs的功能活性。
基于前期基础,研究采用了体外模拟消化和发酵模型来获得PEPs相关肠道消化和肠道菌群酵解产物,进一步研究了相关产物与IMs的相互作用对肠道屏障损伤的潜在保护作用;此外,利用体内动物模型,研究了在DSS 诱导的肠屏障损伤模型中,不同的PEPs摄入时间对其与粘蛋白之间相互作用特征的影响;最后探讨了在IMs介导的情况下,PEPs对肠道屏障损伤的保护作用机制。

研究亮点
1. 采用细胞模型研究PEPs与IMs复合物对肠道屏障损伤的保护作用。
2. 探究PEPs与IMs在体内的相互作用特征,并解析PEPs在IMs的介导下对肠屏障损伤的影响。
3. 评估相互作用特征与肠屏障损伤程度之间的关系,并从消化和发酵的角度研究基于IMs作用下PEPs在肠道中的活性作用机理。
研究结论
IMs和PEPs之间的相互作用会导致PEPs的结构发生变化,从而改变其在肠道中的功能活性作用途径。具体来说,Ims稳态对PEPs改善DSS诱导的肠道屏障损伤影响显著,表现在肠道通透性、粘蛋白和TJs蛋白分泌增加,以及NF-κB和MAPK通路中关键蛋白的磷酸化减少。
图文赏析

图1各组的细胞活力比较(n=8)(A-C)。复合物对炎症因子的影响,消化产物和粘蛋白复合物(D-E);发酵产物和粘蛋白复合物(F-G)。

图2 不同摄入时间的肠粘液和多糖复合物的体内相互作用特征。Zeta 电位(A);粒径(B);荧光光谱(C-F);荧光强度(G)。
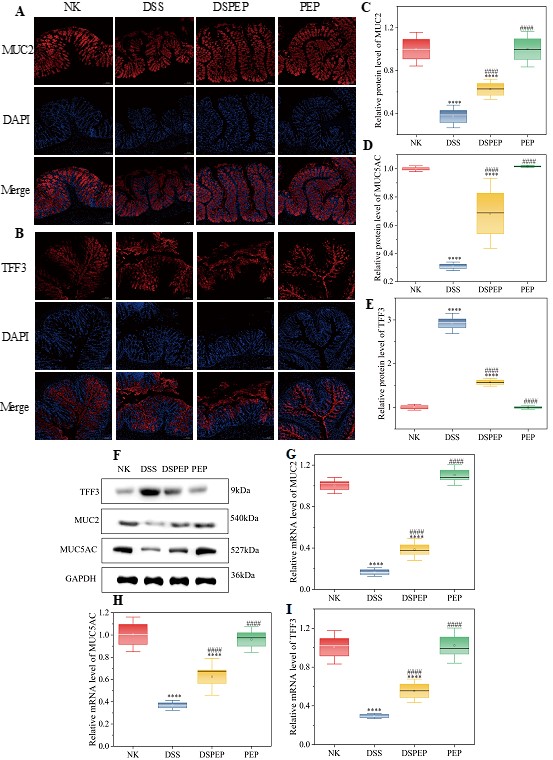
图3 多糖对肠粘液介导的结肠炎中肠道粘蛋白分泌的影响,MUC2(A);TFF3(B);粘蛋白的蛋白水平(C-F);mRNA 水平(G-I)。

图4 ZO-1(A)、occludin(B)和cadherin-1(C)的免疫荧光图像;紧密连接蛋白的免疫印迹分析(D-G)和mRNA表达水平(H-J)。
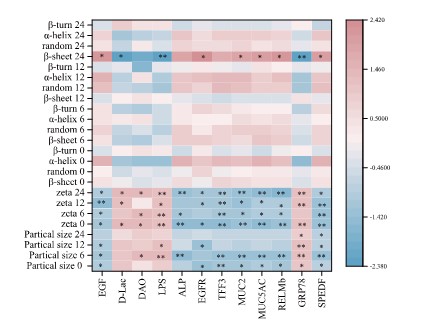
图5 小鼠肠道屏障损伤生物标志物与PEPs和IMs互作特征的相关性分析。
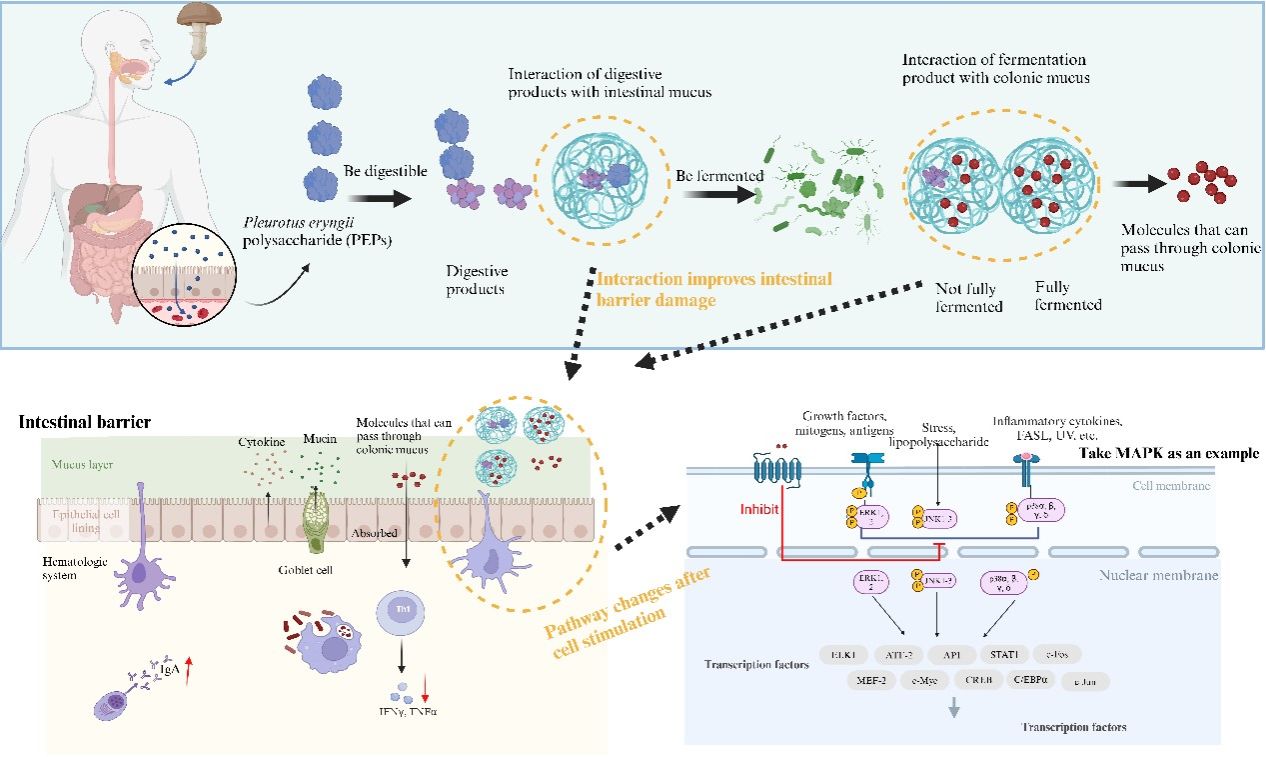
图6 结论可视化剖析图
原文链接:https://pubs.acs.org/doi/10.1021/acs.jafc.4c11339